Este artículo se publicó hace 5 años.
Un modelo de embrión humano para ver en laboratorio lo que pasa en el útero la primera semana
Obtener otros anticonceptivos y evitar la infertilidad son dos de los objetivos de este nuevo desarrollo con células madre.
Malen Ruiz de Elvira
Madrid--Actualizado a
Un modelo del embrión humano en su primera etapa de desarrollo, obtenido en laboratorio, permitirá conocer lo que pasa dentro del útero tras la fecundación y hasta la implantación, con lo que ese conocimiento conlleva. Probablemente permitirá establecer las causas de la infertilidad en muchos casos, desarrollar nuevos anticonceptivos y mejorar las técnicas de reproducción asistida, entre otros objetivos del equipo de investigadores que lo ha presentado.
Se trata de ver en una placa de Petri lo que el embrión hace normalmente escondido en el cuerpo de la mujer, de una forma ética y sin que esto signifique crear vida, aseguran estos científicos del Vienna BioCenter, en Austria.
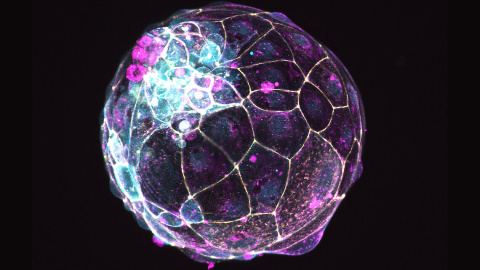
En la primera semana tras la fecundación, los embriones humanos forman una bola de algunos centenares de células que se llama blastocisto y es lo que se implanta en la pared del útero para seguir desarrollándose. Lo que se ha venido intentando es generar análogos del blastocisto, llamados blastoides, a partir de células madre, sin que intervengan ni óvulos ni espermatozoides.
En modelos anteriores presentados se daban algunas limitaciones, como la generación de células de otro tipo al mismo tiempo que algunas de las propias del blastocisto, que son de tres tipos.
Ahora, el equipo dirigido por Nicolas Rivron ha conseguido estimular células madre pluripotentes humanas (derivadas de células adultas) para que se auto organicen de forma fiel y eficiente en modelos realistas de las primeras etapas del desarrollo embrionario, explica el Instituto de Biotecnología Molecular (IMBA), donde se han hecho los experimentos.
Estos blastoides se cultivaron durante 13 días antes de ser destruidos, siguiendo las normas generales para este tipo de trabajos, cuando contenían unas 300 células. Los elementos llegaron a implantarse en células del endometrio también cultivadas in vitro, publican los investigadores en la revista Nature.
Fecundación in vitro
En el futuro, añaden, los blastoides humanos pueden ayudar a identificar dianas terapéuticas y contribuir a mejorar la fecundación in vitro y obtener nuevos anticonceptivos no hormonales. Rivron señala que con este modelo concreto ya han descubierto moléculas que podrían ser anticonceptivos (como uno que solo se tomaría puntualmente) o ayudas a la fertilidad.
Otros científicos que siguen la misma línea de trabajo han señalado que los blastoides no deben ser considerados equivalentes a los blastocistos, o sea, a los embriones humanos, y que se destruyen en el plazo fijado. Eso no evita que surjan continuamente preguntas sobre los aspectos sociales y éticos de estos modelos, que también se pueden utilizar para conocer los efectos de diferentes sustancias químicas sobre las primeras etapas del embrión.
El mayor obstáculo encontrado hasta ahora fue generar el tipo celular destinado a formar la placenta y el nuevo modelo ha conseguido superarlo, indica Magdalena Zernicka-Goetz, de la Universidad de Cambridge. Además, "cuando estos blastoides se cultivan con organoides endometriales que imitan el revestimiento celular natural del útero y se estimulan para favorecer la implantación, modelan las primeras etapas de la interacción del blastocisto con el tejido materno", explica.
Esta científica cree que el modelo se aplicará ampliamente y Rivron que es una alternativa potente y ética al uso en investigación de óvulos humanos fertilizados. Esta línea de trabajo es solo una de las muchas que están haciendo parcialmente realidad las entonces exageradas esperanzas (y también temores) que produjeron la obtención y programación de células madre diez años después de la clonación de la famosa oveja Dolly en 1996, obtenida por la reprogramación de una célula adulta.


Comentarios de nuestros socias/os
¿Quieres comentar?Para ver los comentarios de nuestros socias y socios, primero tienes que iniciar sesión o registrarte.