barcelona
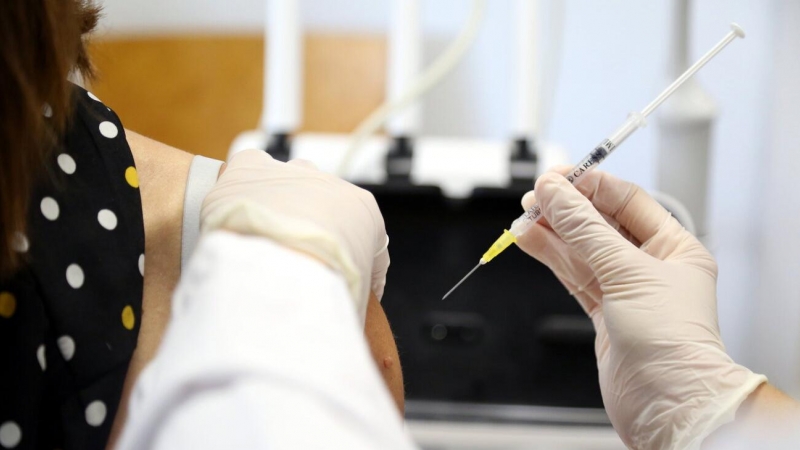
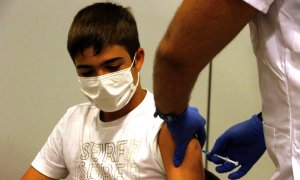
L'Agència Espanyola de Medicaments i Productes Sanitaris (AEMPS) ha autoritzat el primer assaig clínic en humans d'una vacuna contra la Covid-19 desenvolupada a l'Estat espanyol. Es tracta del vaccí PHH-1V dels laboratoris catalans Hipra, segons ha informat aquest dimecres el Ministeri de Sanitat. En l'assaig hi participaran diverses desenes de voluntaris de centres hospitalaris que tinguin entre 18 i 39 anys. Se'ls injectaran dues dosis de la vacuna amb 21 dies de diferència amb l'objectiu d'analitzar la seguretat i tolerabilitat del vaccí així com la seva eficàcia.
La vacuna de la companyia Hipra, amb seu a Amer (Girona), està basada en dues proteïnes recombinants de les variants alfa i beta -plataforma similar a la de Novavax i Sanofi/GSK- que són capaces de generar una resposta immunitària davant d'una de les proteïnes del coronavirus.
L'assaig de fase I/IIa dividirà els voluntaris en grups i anirà augmentant la dosi que rebrà cada grup en funció de la resposta que generi en els primers vaccinats. S'aniran escalant a les dosis següents si no detecten problemes de seguretat, per avaluar quina és la dosi òptima. La farmacèutica gironina preveia que l'estudi clínic comencés a l'agost a l'Hospital Clínic de Barcelona i al Trueta de Girona.
¿Te ha resultado interesante esta noticia?












Comentarios
<% if(canWriteComments) { %> <% } %>Comentarios:
<% if(_.allKeys(comments).length > 0) { %> <% _.each(comments, function(comment) { %>-
<% if(comment.user.image) { %>
![<%= comment.user.username %>]() <% } else { %>
<%= comment.user.firstLetter %>
<% } %>
<% } else { %>
<%= comment.user.firstLetter %>
<% } %>
<%= comment.user.username %>
<%= comment.published %>
<%= comment.dateTime %>
<%= comment.text %>
Responder
<% if(_.allKeys(comment.children.models).length > 0) { %>
<% }); %>
<% } else { %>
- No hay comentarios para esta noticia.
<% } %>
Mostrar más comentarios<% _.each(comment.children.models, function(children) { %> <% children = children.toJSON() %>-
<% if(children.user.image) { %>
![<%= children.user.username %>]() <% } else { %>
<%= children.user.firstLetter %>
<% } %>
<% } else { %>
<%= children.user.firstLetter %>
<% } %>
<% if(children.parent.id != comment.id) { %>
en respuesta a <%= children.parent.username %>
<% } %>
<%= children.user.username %>
<%= children.published %>
<%= children.dateTime %>
<%= children.text %>
Responder
<% }); %>
<% } %> <% if(canWriteComments) { %> <% } %>